Birincil hücreler, dokulardan doğrudan izole edilen hücrelerdir. Sadece normal hücrelerin morfolojisini korumakla kalmaz, aynı zamanda vücuttaki temel biyolojik belirteçleri ve işlevleri de korurlar. Hücre hatlarıyla karşılaştırıldığında, birincil hücrelerin sağladığı deneysel veriler gerçek fizyolojik ortama daha yakındır, bu nedenle biyomedikal araştırmalarda büyük değer taşırlar.

Biyolojik özellikleri temelde değişmediği için, birincil hücreler vücudun büyüme özelliklerini daha doğru bir şekilde simüle edebilir ve moleküler biyoloji, hücre biyolojisi ve proteomik, genomik, hücre araştırması ve genetik araştırma gibi temel biyomedikal araştırmalarda yaygın olarak kullanılmıştır. Aynı zamanda, biyofarmasötikler alanında ideal hücre modelleridir ve hastalık mekanizması araştırmalarında, ilaç taramalarında, ilaç metabolizmasında, toksikoloji değerlendirmesinde, kanser ilacı araştırmalarında ve tedavi geliştirmede yaygın olarak kullanılırlar.
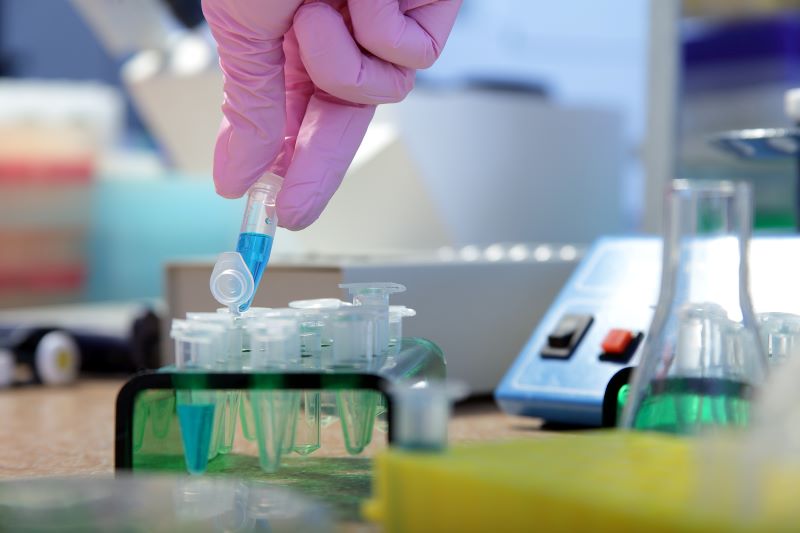
Hücre çıkarma ve in vitro kültür, hücreleri dokulardan veya organlardan izole etme ve uygun koşullar altında kültürleme sürecini ifade eder. Belirli adımlar şunları içerir: steril koşullar altında hedef dokuyu elde etmek, dokuyu tek bir hücre süspansiyonuna ayırmak için tripsin veya kolajenaz gibi sindirim enzimleri kullanmak, ardından hücreleri santrifüjleme, filtreleme vb. ile ayırmak ve son olarak büyümelerini ve işlevlerini sürdürmek için uygun bir kültür ortamında kültürlemek.
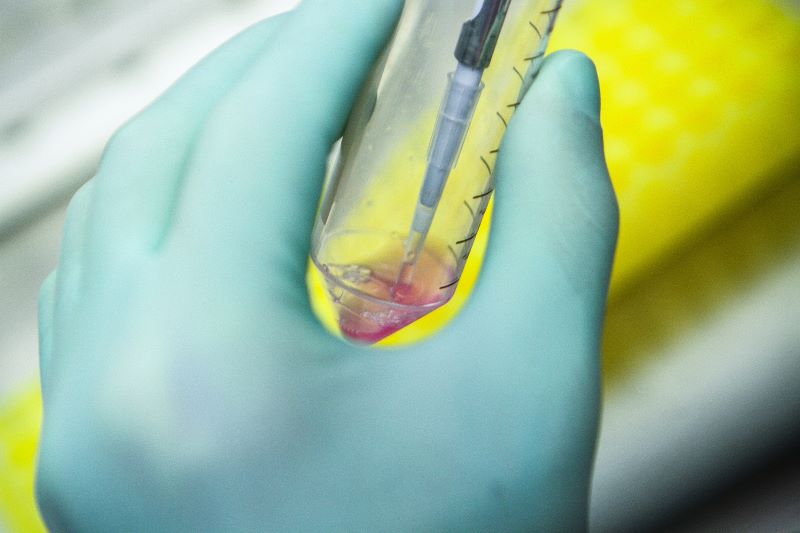
Aşağıda, düşük hızlı soğutmalı santrifüj kullanılarak birincil hücre izolasyonuna yönelik özel adımları paylaşacağız:
Deneysel adımlar (sindirim kültürü yöntemi)
Doku hazırlama ve yıkama
Steril koşullar altında yaklaşık 1 cm³ hedef doku alın, bir tabağa veya behere koyun ve kan kalıntılarını ve bağ dokusunu çıkarmak için uygun miktarda Hanks solüsyonuyla tekrar tekrar yıkayın.

Doku kıyma ve ön işlem
Keskin makas kullanarak dokuyu yaklaşık 0,5 mm × 1 mm boyutlarında küçük parçalara ayırın, tekrar Hanks solüsyonuyla durulayın ve doku parçaları yerleştikten sonra yıkama solüsyonunu atın.
Enzim sindirimi
Doku parçalarını steril bir manyetik karıştırıcı ile önceden takılmış konik bir behere aktarın ve 5-30 mL tripsin veya kolajenaz ekleyin.
Bir lastik tıpa ile sıkıca kapatın ve kalay folyo ile kapatın ve 37°C'lik bir inkübatörde manyetik karıştırıcıya yerleştirin.
Karıştırıcıyı çalıştırın ve eşit şekilde karıştırın. Sindirim süreci sırasında hücre dağılımını gözlemlemek için bir mikroskop kullanın.
Hücrelerin çoğu tek bir duruma ayrıştığında (yaklaşık 10-20 dakika), sindirimi sonlandırmak için hemen uygun miktarda Hanks solüsyonu ekleyin.
Hücre filtrasyonu
Öncelikle sindirilmemiş doku veya büyük hücre kümelerini çıkarmak için 100 μm paslanmaz çelik ağ ile filtreleyin.
Daha sonra nispeten saf tek hücre süspansiyonu elde etmek için 20 μm paslanmaz çelik ağ ile filtreleyin.
Düşük hızlı santrifüjleme ve hücre yıkama
Filtre bir santrifüj tüpüne aktarıldı ve 500 × g'de (yaklaşık 5 dakika) santrifüjlendi.
Üst sıvı atıldı ve hücreler, kalan sindirim enzimlerini gidermek için iki kez Hanks solüsyonuyla yıkandı.
Hücreler serum içeren ortamda yeniden süspanse edildi ve bir hücre süspansiyonu hazırlamak için hafifçe çalkalandı.
Hücre sayımı ve aşılama
Hücre süspansiyonunun konsantrasyonunu saymak ve belirlemek için bir hemositometre kullanın (genellikle 1×10⁵~3×10⁵ hücre/mL).
Hücreleri bir kültür kabına eşit şekilde aşılayın ve 37°C, %5 CO₂ inkübatöründe kültürleyin.
Bu yöntem, son derece canlı birincil hücreleri etkili bir şekilde elde edebilir ve sonraki deneyler için güvenilir bir hücre modeli sağlayabilir. Düşük hızlı soğutmalı santrifüj kullanımı, hücre canlılığını garanti altına alırken birincil hücrelerin ayırma verimliliğini artırmaya yardımcı olabilir ve sonraki deneyler için yüksek kaliteli hücre örnekleri sağlayabilir.
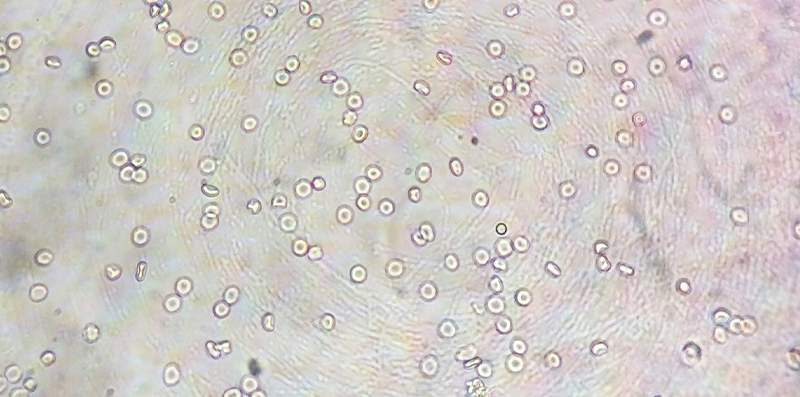
Notlar
Doku durulama
Sindirimden önce, doku bloklarının tripsin ve EDTA üzerindeki kalsiyum, magnezyum iyonları ve serumun inhibitör etkilerini gidermek için 2-3 kez durulanması gerekir.
Doku bloklarını durulama solüsyonunda hafifçe çalkalamak veya karıştırmak için Hanks solüsyonu veya diğer uygun tampon kullanılabilir ve enzim sindiriminin etkisini sağlamak için müdahale eden maddeler tamamen çıkarıldıktan sonra durulama solüsyonu atılabilir.
Sindirim enzimlerinin rolü
Tripsin, pankreas tarafından salgılanan bir proteolitik enzimdir. Esas olarak lizin ve arginini bağlayan peptit bağları üzerinde etki ederek proteinleri daha küçük polipeptitler ve amino asitlere ayırır ve bu da hücrelerin dağılmasına yardımcı olur.
Kolajenaz bakterilerden elde edilir ve kolajeni hidrolize etme konusunda güçlü bir yeteneğe sahiptir. Lifli dokuyu, epitel dokuyu ve hatta bazı kanser dokularını etkili bir şekilde sindirebilir.
Hücre sağkalım oranını iyileştirin
Birincil kültür hücrelerinin ekim yoğunluğunun uygun şekilde artırılması, hücreler arasındaki etkileşimi teşvik edebilir ve onları in vivo büyüme ortamına daha yakın hale getirebilir, böylece hücre sağkalım oranını iyileştirebilir ve yapışmayı ve çoğalmayı teşvik edebilir.
Birincil hücre ayırma deneylerinde santrifüjün temel rolü
Birincil hücre ayırma sürecinde, düşük hızlı soğutmalı santrifüj hayati bir rol oynar, esas olarak hücre zenginleştirme, sindirim enzimleri ve kalıntılarının giderilmesi ve hücre sağkalım oranının iyileştirilmesi için kullanılır. Deneylerdeki temel uygulamaları şunlardır:
Hücre zenginleştirme ve toplama
Sindirimden sonra, doku tek bir hücre süspansiyonuna ayrıştırılır, ancak eksik sindirilmiş doku parçaları, sindirim enzimi kalıntıları ve hücre parçalarıyla karıştırılabilir. Düşük hızlı soğutmalı santrifüjü uygun şekilde ayarlayarak, sağlam hücreler etkili bir şekilde çökeltilebilir, süpernatanttaki enzimler ve artıklar uzaklaştırılabilir ve nispeten saf bir hücre süspansiyonu elde edilebilir.
Kalan sindirim enzimlerini gidermek için hücreleri yıkayın
Tripsin ve kolajenaz gibi sindirim enzimleri hücrelerin normal işlevini etkileyebilir veya hücreler için toksik olabilir. Bu nedenle, ilk santrifüjlemeden sonra hücrelerin serumsuz ortamda veya Hanks solüsyonunda yeniden süspanse edilmesi ve iki kez yıkanması gerekir, her seferinde düşük hızda santrifüjlenir ve kalan enzimlerin çoğunun giderildiğinden ve hücrenin hayatta kalma oranının iyileştirildiğinden emin olmak için üstteki sıvı atılır.
Hücre konsantrasyonu ve kültür koşullarının optimizasyonu
Aşılamadan önce, hücreler aşılama yoğunluğunu artırmak için düşük hızlı santrifüjleme ile daha fazla yoğunlaştırılabilir. Uygun hücre yoğunluğu yalnızca hücre-hücre etkileşimini kolaylaştırmakla kalmaz, aynı zamanda yapışmayı ve çoğalmayı da teşvik ederek birincil hücrelerin hayatta kalma oranını ve kültürün başarı oranını artırır.

Düşük hızlı soğutmalı santrifüjler yalnızca birincil hücrelerin ayrılmasında önemli bir rol oynamakla kalmaz, aynı zamanda hücre kültürü, klinik tıp, biyofarmasötikler, moleküler biyoloji ve kan işleme gibi birçok alanda da yaygın olarak kullanılır. Düşük hızı ve etkili sıcaklık kontrol yetenekleri, onu sıcaklığa duyarlı numune işleme için ideal bir seçim haline getirir. Bir santrifüj kullanırken, santrifüjleme parametreleri ve çalışma prosedürleri, deneyin başarı oranını iyileştirmek ve numunenin bütünlüğünü ve deneysel sonuçların kararlılığını sağlamak için makul şekilde optimize edilmelidir.

Resmi hesabı takip et