Первичные клетки — это клетки, которые непосредственно изолированы из тканей. Они не только сохраняют морфологию нормальных клеток, но и сохраняют ключевые биологические маркеры и функции в организме. По сравнению с клеточными линиями экспериментальные данные, предоставляемые первичными клетками, ближе к реальной физиологической среде, поэтому они имеют большую ценность в биомедицинских исследованиях.

Поскольку их биологические свойства в основном неизменны, первичные клетки могут более точно имитировать характеристики роста организма и широко используются в молекулярной биологии, клеточной биологии и базовых биомедицинских исследованиях, таких как протеомика, геномика, клеточные исследования и генетические исследования. В то же время они также являются идеальными клеточными моделями в области биофармацевтики и широко используются в исследованиях механизмов заболеваний, скрининге лекарств, метаболизме лекарств, оценке токсикологии, исследовании противораковых препаратов и разработке методов лечения.
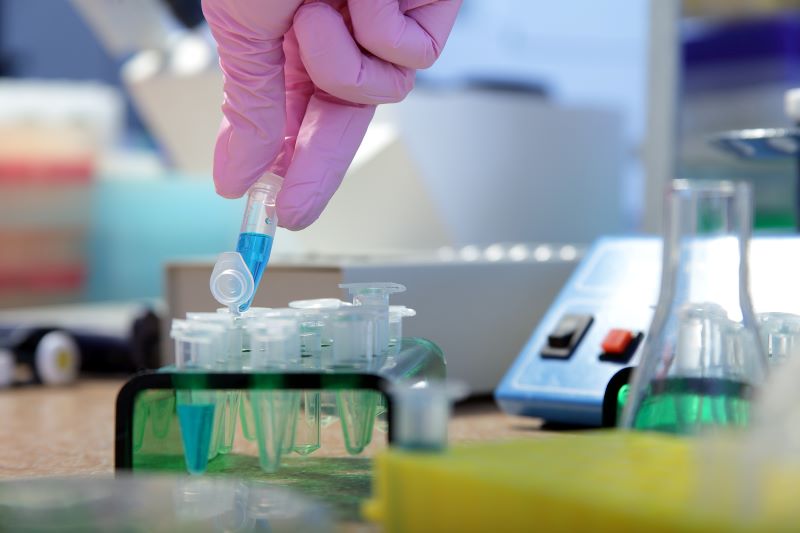
Извлечение клеток и культивирование in vitro относится к процессу изоляции клеток из тканей или органов и их культивирования в соответствующих условиях. Конкретные шаги включают: получение целевой ткани в стерильных условиях, использование пищеварительных ферментов, таких как трипсин или коллагеназа, для диссоциации ткани в суспензию отдельных клеток, затем разделение клеток центрифугированием, фильтрацией и т. д., и, наконец, культивирование их в подходящей культуральной среде для поддержания их роста и функционирования.
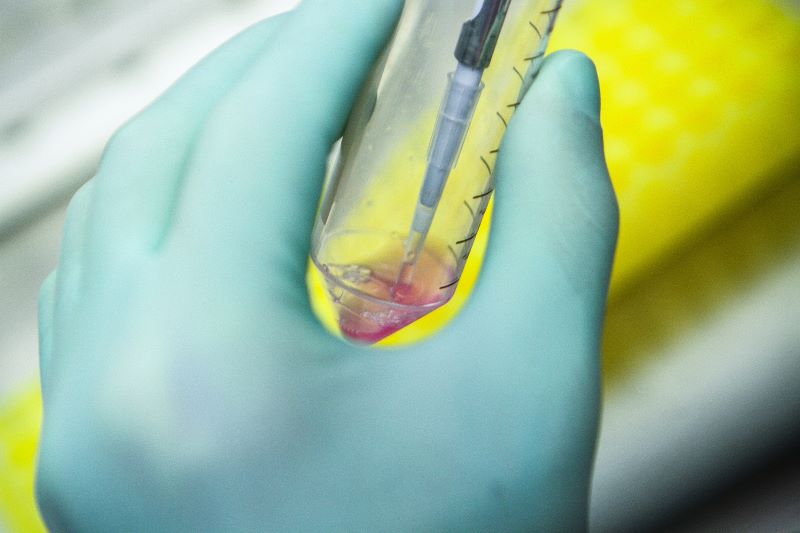
Ниже мы расскажем о конкретных этапах первичной изоляции клеток с использованием низкоскоростной охлаждаемой центрифуги:
Экспериментальные этапы (метод культивирования с помощью переваривания)
Подготовка и промывание ткани
В стерильных условиях возьмите около 1 см³ целевой ткани, поместите ее в чашку или стакан и несколько раз промойте соответствующим количеством раствора Хэнкса, чтобы удалить остатки крови и соединительной ткани.

Измельчение и предварительная обработка тканей
Острыми ножницами измельчите ткань на мелкие кусочки размером примерно 0,5 мм × 1 мм, снова промойте раствором Хенкса и слейте промывочный раствор после того, как кусочки ткани осядут.
Ферментативное пищеварение
Перенесите кусочки ткани в конический стакан, предварительно оснащенный стерильной магнитной мешалкой, и добавьте 5–30 мл трипсина или коллагеназы.
Плотно закройте резиновой пробкой, запечатайте фольгой и поместите на магнитную мешалку в инкубатор с температурой 37 °C.
Включите мешалку и равномерно перемешайте. Используйте микроскоп для наблюдения за дисперсией клеток в процессе переваривания.
Когда большинство клеток диссоциируют в единое состояние (примерно через 10–20 минут), немедленно добавьте соответствующее количество раствора Хэнкса, чтобы завершить переваривание.
Фильтрация клеток
Сначала отфильтруйте с помощью сетки из нержавеющей стали с размером ячеек 100 мкм, чтобы удалить непереваренную ткань или крупные скопления клеток.
Затем отфильтруйте с помощью сетки из нержавеющей стали с размером ячеек 20 мкм, чтобы получить относительно чистую суспензию отдельных клеток.
Низкоскоростное центрифугирование и промывание клеток
Фильтрат переносили в центрифужную пробирку и центрифугировали при 500×g (около 5 минут).
Супернатант удаляли, а клетки дважды промывали раствором Хэнкса для удаления остаточных пищеварительных ферментов.
Клетки ресуспендировали в среде, содержащей сыворотку, и осторожно встряхивали для приготовления клеточной суспензии.
Подсчет клеток и инокуляция
Используйте гемоцитометр для подсчета и определения концентрации клеточной суспензии (обычно 1×10⁵~3×10⁵ клеток/мл).
Равномерно инокулируйте клетки в чашку для культивирования и культивируйте в инкубаторе при 37°C, 5% CO₂.
Этот метод позволяет эффективно получать высокожизнеспособные первичные клетки и обеспечивать надежную модель клеток для последующих экспериментов. Использование низкоскоростной охлаждаемой центрифуги может помочь повысить эффективность разделения первичных клеток, обеспечивая при этом жизнеспособность клеток, предоставляя высококачественные образцы клеток для последующих экспериментов.
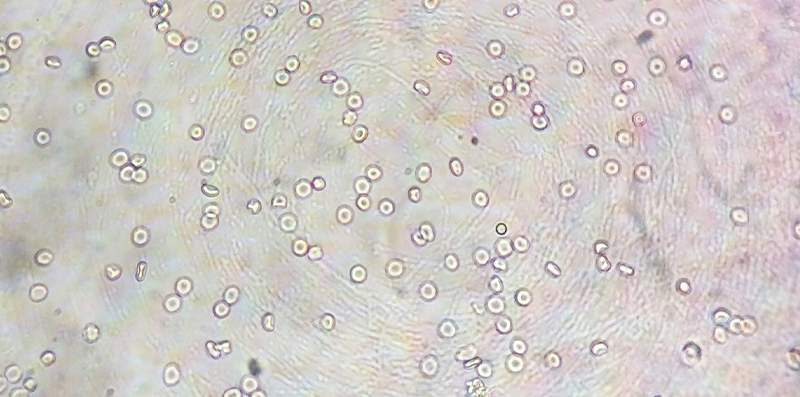
Примечания
Промывание тканей
Перед перевариванием тканевые блоки необходимо промыть 2–3 раза, чтобы удалить ингибирующее действие ионов кальция, магния и сыворотки на трипсин и ЭДТА.
Можно использовать раствор Хэнкса или другой подходящий буфер для осторожного встряхивания или перемешивания тканевых блоков в промывочном растворе, а промывочный раствор можно вылить после полного удаления мешающих веществ, чтобы обеспечить эффект ферментативного переваривания.
Роль пищеварительных ферментов
Трипсин — протеолитический фермент, секретируемый поджелудочной железой. Он в основном действует на пептидные связи, соединяющие лизин и аргинин, расщепляя белки на более мелкие полипептиды и аминокислоты, что помогает клеткам рассеиваться.
Коллагеназа получена из бактерий и обладает сильной способностью гидролизовать коллаген. Она может эффективно переваривать фиброзную ткань, эпителиальную ткань и даже некоторые раковые ткани.
Улучшить выживаемость клеток
Правильное увеличение плотности посева клеток первичной культуры может способствовать взаимодействию между клетками и приблизить их к среде роста in vivo, тем самым улучшая выживаемость клеток и способствуя адгезии и пролиферации.
Ключевая роль центрифуги в экспериментах по первичному разделению клеток
В процессе первичного разделения клеток низкоскоростная охлаждаемая центрифуга играет важную роль, в основном используемая для обогащения клеток, удаления пищеварительных ферментов и мусора, а также повышения выживаемости клеток. Ее основные применения в экспериментах включают:
Обогащение и сбор клеток
После переваривания ткань будет диссоциирована в суспензию отдельных клеток, но она может быть смешана с не полностью переваренными фрагментами тканей, остатками пищеварительных ферментов и фрагментами клеток. При правильной настройке низкоскоростной охлаждаемой центрифуги можно эффективно осадить целые клетки, удалить ферменты и дебрис в супернатанте и получить относительно чистую суспензию клеток.
Промойте клетки, чтобы удалить остаточные пищеварительные ферменты
Пищеварительные ферменты, такие как трипсин и коллагеназа, могут влиять на нормальную функцию клеток или даже быть токсичными для клеток. Поэтому после первого центрифугирования клетки необходимо ресуспендировать в бессывороточной среде или растворе Хэнкса и дважды промыть, каждый раз центрифугируя на низкой скорости и сливая супернатант, чтобы гарантировать удаление большей части остаточных ферментов и повысить выживаемость клеток.
Концентрация клеток и оптимизация условий культивирования
Перед инокуляцией клетки можно дополнительно концентрировать с помощью низкоскоростного центрифугирования для увеличения плотности инокуляции. Соответствующая плотность клеток не только облегчает взаимодействие клеток, но и способствует адгезии и пролиферации, тем самым увеличивая выживаемость первичных клеток и успешность культивирования.

Низкоскоростные охлаждаемые центрифуги не только играют ключевую роль в разделении первичных клеток, но и широко используются во многих областях, таких как клеточная культура, клиническая медицина, биофармацевтика, молекулярная биология и обработка крови. Низкая скорость и эффективные возможности контроля температуры делают их идеальным выбором для обработки образцов, чувствительных к температуре. При использовании центрифуги параметры центрифугирования и рабочие процедуры должны быть разумно оптимизированы для повышения успешности эксперимента и обеспечения целостности образца и стабильности экспериментальных результатов.

Посмотреть Публичный номер.