As células primárias são células que estão diretamente isoladas dos tecidos. Não só mantêm a morfologia das células normais, como também retêm os principais marcadores biológicos e funções do organismo. Comparativamente com as linhas celulares, os dados experimentais fornecidos pelas células primárias estão mais próximos do ambiente fisiológico real, sendo, por isso, de grande valor na investigação biomédica.

Uma vez que as suas propriedades biológicas permanecem basicamente inalteradas, as células primárias podem simular com maior precisão as características de crescimento do corpo e têm sido amplamente utilizadas em biologia molecular, biologia celular e investigação biomédica básica, como proteómica, genómica, investigação celular e investigação genética. Ao mesmo tempo, são também modelos celulares ideais no campo dos produtos biofarmacêuticos e são amplamente utilizados na investigação sobre mecanismos de doenças, rastreio de medicamentos, metabolismo de medicamentos, avaliação toxicológica, investigação de medicamentos contra o cancro e desenvolvimento de tratamentos.
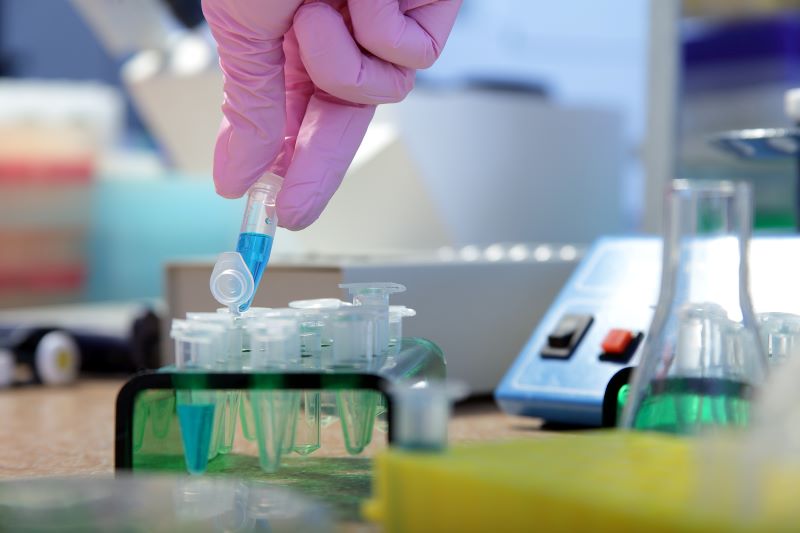
A extração de células e a cultura in vitro referem-se ao processo de isolar células de tecidos ou órgãos e cultivá-las em condições apropriadas. As etapas específicas incluem: obter o tecido alvo em condições estéreis, utilizar enzimas digestivas como a tripsina ou a colagenase para dissociar o tecido numa única suspensão de células, depois separar as células por centrifugação, filtração, etc.
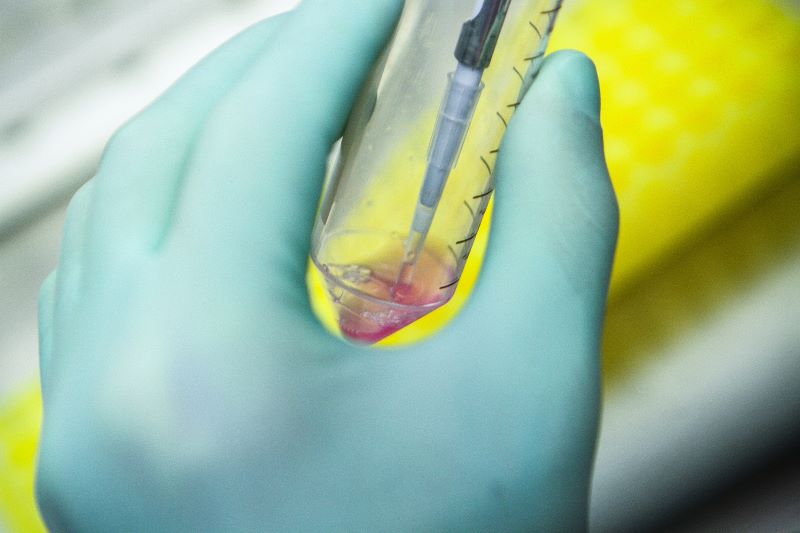
Abaixo, partilharemos as etapas específicas para o isolamento primário de células utilizando uma centrífuga refrigerada de baixa velocidade:
Etapas experimentais (método de cultura de digestão) Preparação e lavagem do tecido Retire cerca de 1 cm³ do tecido alvo em condições estéreis, coloque-o numa placa ou gobelé e enxague-o repetidamente com uma quantidade apropriada de solução de Hanks para remover os resíduos de sangue e tecido conjuntivo.

Trituração e pré-tratamento do tecido Utilize uma tesoura afiada para picar o tecido em pequenos pedaços de aproximadamente 0,5 mm × 1 mm, volte a enxaguar com solução de Hanks e elimine a solução de lavagem após os pedaços de tecido terem assentado.
Digestão enzimática Transfira os pedaços de tecido para um gobelé cónico pré-instalado com um agitador magnético estéril e adicione 5-30 mL de tripsina ou colagenase.
Cubra bem com uma rolha de borracha, sele com papel de alumínio e coloque num agitador magnético numa incubadora a 37 °C.
Ligue o misturador e misture uniformemente. Utilize um microscópio para observar a dispersão celular durante o processo de digestão.
Quando a maioria das células estiver dissociada num único estado (cerca de 10 a 20 minutos), adicione imediatamente uma quantidade apropriada de solução de Hanks para terminar a digestão.
Filtração celular Primeiro, filtre com uma malha de aço inoxidável de 100 μm para remover tecido não digerido ou grandes aglomerados de células.
Em seguida, filtre com uma malha de aço inoxidável de 20 μm para obter uma suspensão de células individuais relativamente pura.
Centrifugação a baixa velocidade e lavagem das células O filtrado foi transferido para um tubo de centrífuga e centrifugado a 500×g (cerca de 5 minutos).
O sobrenadante foi rejeitado e as células foram lavadas duas vezes com solução de Hanks para remover as enzimas digestivas residuais.
As células foram ressuspendidas em meio contendo soro e agitadas suavemente para preparar uma suspensão celular.
Contagem de células e inoculação Utilize um hemocitómetro para contar e determinar a concentração da suspensão celular (geralmente 1×10⁵~3×10⁵ células/mL).
Inocule uniformemente as células numa placa de cultura e cultive numa incubadora a 37°C e 5% de CO₂.
Este método pode obter eficazmente células primárias altamente viáveis e fornecer um modelo celular fiável para experiências subsequentes. A utilização de uma centrífuga refrigerada de baixa velocidade pode ajudar a melhorar a eficiência de separação das células primárias, garantindo a viabilidade celular e fornecendo amostras de células de alta qualidade para experiências subsequentes.
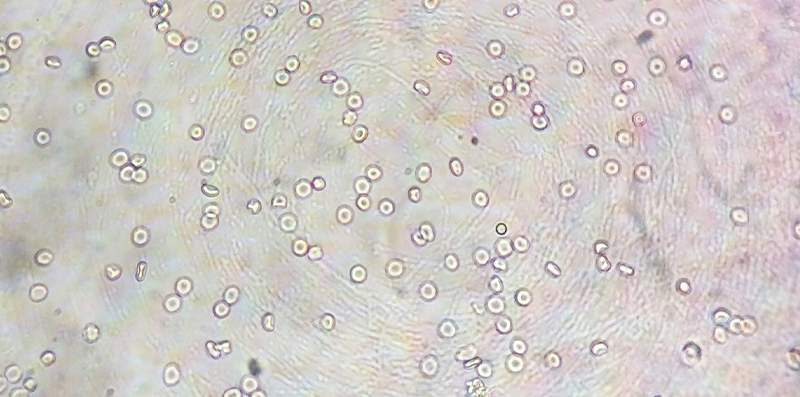
Notas
Enxaguamento do tecido Antes da digestão, os
blocos de tecido necessitam de ser enxaguados 2 a 3 vezes para remover os efeitos inibitórios do cálcio, dos iões de magnésio e do soro sobre a tripsina e o EDTA.
A solução de Hanks ou outro tampão apropriado pode ser utilizado para agitar ou mexer suavemente os blocos de tecido na solução de enxaguamento, e a solução de enxaguamento pode ser eliminada após as substâncias interferentes serem totalmente removidas para garantir o efeito da digestão enzimática.
O papel das enzimas digestivas
A tripsina é uma enzima proteolítica segregada pelo pâncreas. Atua principalmente nas ligações peptídicas que ligam a lisina e a arginina, decompondo as proteínas em polipeptídeos mais pequenos e aminoácidos, o que ajuda as células a dispersarem.
A colagenase é derivada de bactérias e tem uma forte capacidade de hidrolisar o colagénio. Pode digerir eficazmente o tecido fibroso, o tecido epitelial e até mesmo alguns tecidos cancerígenos.
Melhora a taxa de sobrevivência celular
Aumentar adequadamente a densidade de sementeira das células de cultura primária pode promover a interação entre as células e torná-las mais próximas do ambiente de crescimento in vivo, melhorando assim a taxa de sobrevivência celular e promovendo a adesão e a proliferação.
O papel fundamental da centrífuga nas experiências primárias de separação de células
No processo de separação primária de células, a centrifugadora refrigerada de baixa velocidade desempenha um papel vital, sendo utilizada principalmente para o enriquecimento celular, remoção de enzimas digestivas e detritos e melhoria da taxa de sobrevivência celular. As suas principais aplicações em experiências incluem:
Enriquecimento e colheita de células
Após a digestão, o tecido será dissociado numa única suspensão celular, mas poderá ser misturado com fragmentos de tecido incompletamente digeridos, resíduos de enzimas digestivas e fragmentos de células. Ao configurar corretamente a centrífuga refrigerada de baixa velocidade, as células intactas podem ser precipitadas de forma eficaz, as enzimas e os resíduos no sobrenadante podem ser removidos e pode ser obtida uma suspensão de células relativamente pura.
Lave as células para remover as enzimas digestivas residuais
As enzimas digestivas como a tripsina e a colagenase podem afetar a função normal das células ou até ser tóxicas para as mesmas. Portanto, após a primeira centrifugação, as células precisam de ser ressuspensas em meio sem soro ou solução de Hanks e lavadas duas vezes, cada vez centrifugadas a baixa velocidade e o sobrenadante descartado para garantir que a maioria das enzimas residuais são removidas e a taxa de sobrevivência celular é melhorada.
Concentração celular e otimização das condições de cultura
Antes da inoculação, as células podem ser ainda mais concentradas por centrifugação a baixa velocidade para aumentar a densidade da inoculação. A densidade celular adequada não só facilita a interação célula a célula, como também promove a adesão e a proliferação, aumentando assim a taxa de sobrevivência das células primárias e a taxa de sucesso da cultura.

As centrífugas refrigeradas de baixa velocidade não só desempenham um papel fundamental na separação de células primárias, como também são amplamente utilizadas em muitos campos, tais como cultura celular, medicina clínica, biofármacos, biologia molecular e processamento de sangue. A sua baixa velocidade e as suas eficientes capacidades de controlo de temperatura tornam-no a escolha ideal para o processamento de amostras sensíveis à temperatura. Quando se utiliza uma centrífuga, os parâmetros de centrifugação e os procedimentos operacionais devem ser razoavelmente otimizados para melhorar a taxa de sucesso da experiência e garantir a integridade da amostra e a estabilidade dos resultados experimentais.

Seguir a conta oficial